Existe atualmente uma forma de corrigir, substituir e até mesmo apagar um DNA problemático. Conheça a ciência por detrás disto, os riscos e aquilo que o futuro pode trazer.
O que é, afinal, a edição genética?
Os cientistas comparam-na ao recurso de busca e substituição, usado no Word para corrigir erros ortográficos em documentos escritos no computador. A diferença é que, ao invés de corrigir palavras, a edição genética torna possível a reescrita do nosso ADN, um código biológico que funciona como uma espécie de “manual de instruções” de qualquer organismo vivo. Através da edição genética os investigadores podem hoje desativar determinados genes, corrigir periogosas mutações e, inclusivé, alterar a atividade de alguns genes em plantas, animais e seres humanos.
Qual o objetivo?
Muita da euforia em torno da edição genética está diretamente relacionada com o seu potencial para tratar e prevenir doenças no Ser Humano. Existem, atualmente, milhares de alterações genéticas que podem ser passadas de geração em geração, sendo, muitas delas, alterações que podem vir a manifestar-se nocivas e debilitantes. Não falamos de casos raros: uma em cada 25 crianças nasce com uma alteração genética. Entre as mais comuns encontram-se a fibrose quística, a anemia falciforme e distrofia muscular. A edição genética parece transportar consigo a promessa de tratar algumas destas alterações através da reescrita do ADN “defeituoso” nas células destes pacientes. No entanto, a edição genética pode fazer muito mais do que emendar genes “defeituosos”. A técnica está a ser atualmente utilizada também para modificar as células imunes e, assim, ajudar a combater o cancro ou a potenciar a resistência ao HIV. Entre as utilizações está também o uso da terapia genética para corrigir genes em embriões, e, deste modo, prevenir os recém-nascidos de vir a desenvolver doenças graves. Trata-se, no entanto, de um tema controverso uma vez que a edição genética afeta os espermatozóides e as células do ovo o que significa que, a longo prazo, podem existir efeitos colaterais para as gerações futuras.
Para que mais pode servir a alteração genética?
A indústria agrícola tem vindo a servir-se da edição genética por uma série de razões. Torna o procedimento mais rápido, mais barato e mais preciso e traz ainda aos produtores o benefício de melhorar as suas colheitas sem necessidade de adicionar genes provenientes de outros organismos.
A edição genética tornou possível fazer tomates sem grainhas, trigo sem glúten e cogumelos que não escurecem quando ficam velhos.
No entanto, também outros ramos da medicina sem têm servido da técnica para aproveitar o seu potencial. Um conjunto de empresas tem vindo a desenvolver antibióticos de última geração que trabalham com vírus inofensivos para atacar estirpes específicas de bactérias que causam infecções perigosas para o organismo. No entretanto, alguns investigadores estão a usar a edição genética para tornar mais segura a transplantação de órgãos de animais (como o porco, por exemplo) para os seres humanos.
No campo da investigação, a edição genética transformou a investigação fundamental, ajudando os cientistas a compreender, de modo mais preciso, como funcionam determinados genes.
Como funciona?
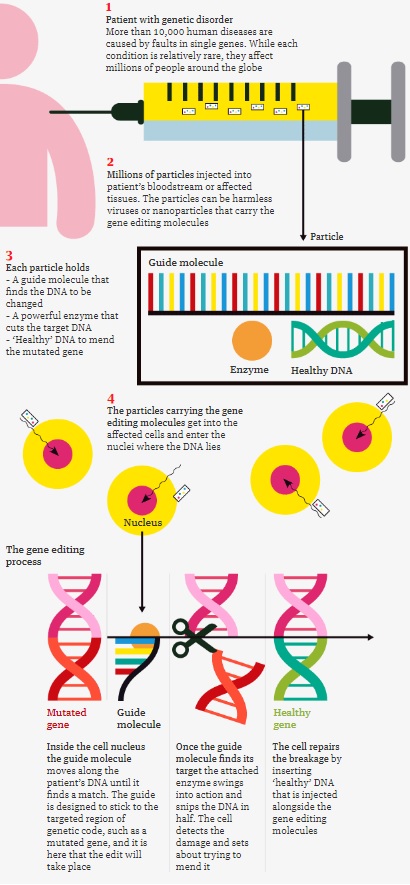
Há muitas formas de editar genes, mas, o maior avanço nos últimos anos é uma ferramenta chamada Crispr-Cas9. Esta ferramenta serve-se de uma molécula guia (o bit Crispr) para encontrar uma região específica no código genético – um gene mutado, por exemplo – que é, posteriormente, cortado por uma enzima (Cas9).
Quando a célula tenta corrigir os danos provoca, normalmente, uma confusão terrível, e desativa o gene. Isto, em si, torna-se útil para desligar genes nocivos.
No entanto, outro tipo de correcções são possíveis. Para corrigir um gene “defeituoso” os cientistas podem, por exemplo, cortar o DNA mutado e substitui-lo por uma sequência saudável que é injetada, em simultâneo, com as moléculas de Crispr-Cas9. Ao invés do Cas9 podem ser usadas diferentes enzimas como a Cpf1, que pode ajudar a editar o DNA de forma mais efetiva.
O que são, afinal, os genes?
Os genes são os modelos biológicos que o corpo usa para produzir proteínas e enzimas estruturais, essenciais para construir e manter tecidos e órgãos. São feitas de sequências de código genético denominados pelas letras G,C,T e A. Os seres humanos têm cerca de 20.000 genes agrupados em 23 pares de cromossomas, todos enrolados no núcleo de quase todas as células do corpo humano. Apenas cerca de 1,5% do nosso código genético, ou genoma, é composto por genes. Os outros 10% regulam-nos, garantindo que estes se ligam e desligam, nas células certas e nos momentos exatos. O resto do nosso DNA é, aparentemente, inútil. “A maioria do nosso genoma não serve para nada”, diz Gerton Lunter, geneticista na Universidade de Oxford. “É simplesmente detrito evolutivo”.
Mas, como chegam às células certas?
Este é o grande desafio. Muitas drogas são compostas por moléculas pequenas que podem ser transportadas através da corrente sanguínea e entregues a órgãos e tecidos durante esse caminho. As moléculas resultantes da edição de genes são enormes, em comparação com as outras, e têm, normalmente, mais problemas para entrar nas células. No entanto, é possível faze-las entrar. Uma forma é empacotar estas moléculas editadas transformando-as em vírus inofensivos que infetam determinados tipos de células. Então, milhares deles são injetados na corrente sanguínea ou entregues, diretamente, nos tecidos afetados.
Uma vez dentro do corpo, os vírus invadem as células-alvo e libertam as moléculas editadas para que possam fazer o seu trabalho.
Em 2017, no Texas, os cientistas usaram esta abordagem para tratar, em ratos, a distrofia muscular de Duchenne. O próximo passo é testar a abordagem em humanos.
Mas, os vírus não são a única forma de o fazer. Os investigadores têm vindo a usar nanopartículas de gordura para transportar as moléculas Crispr-Cas9 para o fígado, bem como pequenas descargas de electricidade para abrir os poros em embriões permitindo a entrada da moléculas editadas.
Este procedimento tem de ser feito no corpo?
Não. Em alguns dos primeiros ensaios com edição genética, os cientistas coletaram células do sangue do paciente, efetuando as alterações genéticas necessárias, e injetando as células modificadas de volta ao organismo dos pacientes. Trata-se de um procedimento que parece ser promissor, sobretudo, para o tratamento de pessoas com HIV. Quando o vírus entra no corpo, infecta e mata as células imunes. Mas, para o fazer, o HIV tem, necessariamente, de ser ligar a proteínas específicas na superfície das células imunes. Neste sentido, os cientistas recolheram um conjunto de células imunes do sangue do paciente e usaram a edição genética para cortar o DNA de que as células precisavam para produzir essas proteínas de superfície. Sem estas proteínas, o vírus fica impedido de entrar nas células.
Uma abordagem semelhante pode também ser usada para combater determinados tipos de cancro: as células imunes são coletadas do sangue do paciente e são editadas de modo a produzir proteínas de superfície que se ligam a células cancerígenas e as matam.
Tendo editado as células de forma a torná-las “assassinas do cancro”, os cientistas trabalham agora em conjuntos massivos de células que serão, posteriormente, reintroduzidas no corpo do paciente.
A magia de modificar células fora do corpo é que estas podem ser verificadas antes de ser reintroduzidas no paciente, garantindo que o processo de edição correu da forma mais adequada.
O que é que pode correr mal ?
A edição genética moderna é bastante precisa mas não é infalível. O procedimento pode falhar, atingindo umas células, mas, revelando-se incapaz de chegar a outras. Mesmo quando a Crispr chega onde é preciso, a edição pode diferir de célula para célula, emendando, por exemplo, duas cópias de um gene mutado numa determinada célula mas, eventualmente, apenas uma em outra célula.
Para algumas doenças genéticas este dado pode não ser muito relevante, mas, para outras, apenas um gene mutado por causar a doença.
Outro problema acontece quando a edição é feita no local errado do genoma. Pode haver centenas de edições “fora do alvo” que se podem tornar perigosas se interromperem a atividade dos genes saudáveis ou o DNA regulatório.
Conduzir-nos-á isto a uma nova forma de criar bebés?
Até agora a medicina tem feito um esforço hérculeo que visa reduzir os genes “defeituosos” tanto em crianças como em adultos. No entanto, um par de estudos mostrou ser possível corrigir perigosas mutações também em embriões. Em 2017, um conjunto de cientistas convocados pela Academia Nacional de Ciências e de Medicina dos Estados Unidos, aprovaram, com cautela, a edição genética em embriões humanos com o objetivo de prevenir o aparecimento de doenças mais graves. No entanto, o procedimento apenas por uma vez mostrou ser seguro.
Qualquer edição feita em embriões vai afetar todas as células da pessoa e isso será passado, posteriormente, aos seus filhos, motivo pelo qual é crucial evitar erros que possam ser prejudiciais bem como quaisquer efeitos colaterais.
Esta “engenharia de embriões humanos” levanta também a perspetiva desconcertante de podermos vir a ter “bebés por medida”, ou seja, crianças em que os embriões são alterados por razões que nada têm que ver com medicina. Tornar uma pessoa mais inteligente, mais alta, com mais massa muscular, são algumas das hipóteses. Traços como estes podem envolver a edição de milhares de genes, muitos deles desconhecidos.
Assim, por enquanto, os “bebés por medida” são apenas uma perspetiva distante.
Quando estará a edição genética disponível para os pacientes?
A questão reside, atualmente, em transportar a edição genética para a clínica. De momento, estão em curso cerca de uma dúzia de ensaios com o Crispr-Cas9, a maioria deles conduzidos por investigadores chineses por forma a combater determinados tipos de cancro. Um dos primeiros foi lançado em 2016, quando os médicos da província de Sichuan, administraram células imunes a um paciente num estadio evoluído da doença.
Nos próximos anos espera-se que aumente o número de ensaios na América e na Europa.
Source: The Guardian, by Ian Sample
O que é? Qual o objetivo? Para que mais pode servir? Como é que funciona? Qual o futuro? Saiba tudo sobre edição genética ou como reescrever o código da vida.